이로써 향후 유방암, 자궁암 등의 항암효과를 배가시킬 수 있는 가능성이 열렸다.
연세대 송재환 교수(45세)와 이은우 박사가 주도한 이번 연구는 교육과학기술부(장관 이주호)와 한국연구재단(이사장 이승종)이 추진하는 중견연구자지원사업(도약연구)의 지원으로 수행되었고, 세계 최고 과학전문지 ‘네이처’의 온라인 자매지인 ‘Nature Communications(네이처 커뮤니케이션)’최신호(7월 31일자)에 게재됐다.
세포사멸수용체는 다양한 세포에서 발견되며 외인성세포사멸을 일으키는 주요 단백질이다. 대표적인 세포사멸수용체에는 TNFR, FAS, TRAILR이 있으면 각각의 리간드인 TNF, FAS ligand, TRAIL과의 결합을 통해 활성화 되어 세포사멸을 일으킨다.
세포사멸 수용체는 면역세포에서 발달되어 있는데, 면역반응시 순간적으로 많은 양의 면역세포를 생성한 후, 면역반응이 끝났을 때 면역세포를 효율적으로 제거하기 위한 수단으로 세포사멸 수용체를 이용하게 된다.
세포사멸 수용체의 한 종류인 트레일(TRAIL)은 정상세포에 독성은 없지만, 암세포를 효율적으로 제거할 수 있는 특징이 있어서 트레일을 이용한 항암치료에 대한 연구가 활발히 진행되고 있다.
송재환 교수 연구팀은 FADD(파드) 단백질을 분해하는 원리를 처음으로 규명하여, MKRN1(마코린 원) 단백질을 통해 FADD 단백질의 활성을 조절하는데 성공했다.
송 교수팀은 MKRN1 단백질이 FADD 단백질의 유비퀴틴화*를 유도함으로써 FADD 단백질의 분해를 촉진하여 암세포를 사멸한다는 사실을 밝혀냈다.
특히 연구팀은 유방암과 자궁암 환자 샘플에서 MKRN1 단백질의 양이 정상세포에 비해 암세포에서 증가되었고, 반면에 FADD 단백질은 암세포에서 감소했음을 확인했다.
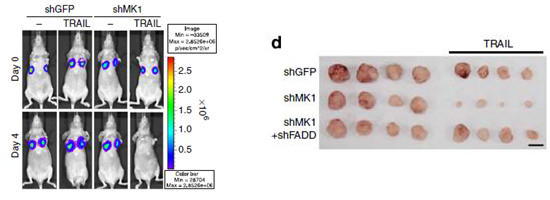
또한 연구팀은 유방암과 자궁암 세포주*에서 MKRN1의 기능을 억제하면 FADD 단백질의 양이 증가하여, FADD 단백질이 많은 세포주에 약물(TRAIL)로 항암치료를 하면 종양이 더욱 빠르게 감소하는 등 치료효과가 크게 증가한다는 사실을 동물실험(생쥐)을 통해 검증했다.
유비퀴틴 접합효소(ubiquitin ligase)는 특정 단백질에 유비퀴틴을 연결하는 단백질로 약 수백종류가 알려져 있다. 마코린1은 유비퀴틴 접합효소에 속한 단백질로서 대표적으로 텔로머라아제(telomerase)와 p53 암억제 단백질에 유비퀴틴화를 유도하고 단백질의 분해를 일으키는 것으로 알려져 있다.
송재환 교수는 “지금까지 외인성 세포사멸과 관련하여 FADD에 대한 연구가 활발히 진행되지 못했는데, 이번 연구성과는 FADD 단백질의 분해원리를 처음으로 밝혀, MKRN1 활성 저해제를 개발하면 다른 항암요법과 병행하여 치료효과를 획기적으로 높일 수 있을 것으로 기대한다”고 연구의의를 밝혔다.
'시민과 공감하는 언론 일요주간에 제보하시면 뉴스가 됩니다'
▷ [전화] 02–862-1888
▷ [메일] ilyoweekly@daum.net
[저작권자ⓒ 일요주간. 무단전재-재배포 금지]





























































![부산 덕포동 중흥S클래스 건설현장서 화재 발생...검은 연기 치솟아 [제보+]](/news/data/20220901/p1065590204664849_658_h2.jpg)
![[포토] 제주 명품 숲 사려니숲길을 걷다 '한남시험림'을 만나다](/news/data/20210513/p1065575024678056_366_h2.png)
![[포토] 해양서고 예방·구조 위해 '국민드론수색대'가 떴다!](/news/data/20210419/p1065572359886222_823_h2.jpg)
![[언택트 전시회] 사진과 회화의 경계](/news/data/20210302/p1065575509498471_939_h2.jpg)











